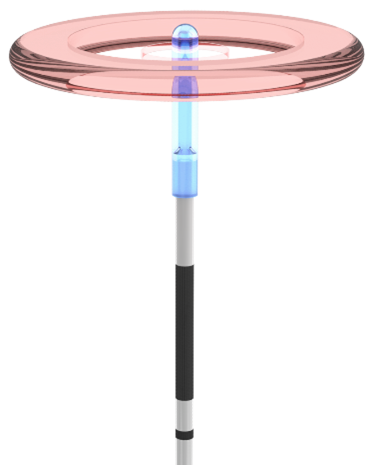
Fibres laser à émission radiale – Ringlight®
Les fibres Ringlight® sont des dispositifs médicaux destinées au traitement de varices, par laser endoveineux. Elles permettent un positionnement optimal du faisceau laser vers son champ thérapeutique cible : la paroi veineuse.
Conçues et développées par LSO Medical, les fibres laser à émission radiale Ringlight® permettent une diffusion optimale de l’énergie pour une ablation plus sûre et efficace :
- Connecteur fibre SMA 905 : connecteur de référence
- Corps de fibre Si/Si pour une transmission optimale de l’énergie
- Marquage à 360° sur la longueur des fibres pour un dosage exact de l’énergie et de la vitesse de retrait.
- Pointe de fibre à émission radiale, à 360° : 100 % de l’énergie est diffusée vers la paroi veineuse.
- Pointe de fibre encapsulée et arrondie
– pour réduire le risque de perforation de la veine
– échogène et facile à localiser par ultrasons - Monitoring Back Reflection, pour un monitoring temps réel de la délivrance effective en bout de fibre.
- Carte à puce pour un suivi patient optimal.

Disponible en diamètre de noyau de 400 μm ou 600 μm. Un matériau de haute qualité permet de réduire l’énergie et d’améliorer la transillumination du faisceau de visée pendant le fonctionnement.
La fibre laser Ringlight_SB® est la nouvelle génération de fibre radiale LSO Medical, compatibles SnakeBack®.
La technologie SnakeBack® : SnakeBack® est un système de retrait assisté sans tension, capable de planifier, d’appliquer et de surveiller l’apport d’énergie dans la veine.
Les fibres Ringlight_SB® reprennent le design et la qualité de production des fibres Ringlight®.

- Longueur totale : 2,5 m
- Indicateur 1 : retrait de l’introducteur
- Indicateur 2 : arrêt de la procédure
- Marquages centimétriques et décimétriques
Références de commande et points techniques
LSO Medical vous propose une solution clé en main, pour lancer une activité endoveineuse thermique.
Vous souhaitez échanger autour de votre projet d’activité ? Contactez-nous.
a) Fibre laser Ringlight_SB®
| Libellé | Référence | Spécifications techniques | Compatibilités |
|---|---|---|---|
| RINGLIGHT® FIBER PROBE IR_SB 1,8 mm CE 1639 | ORLF000003_SB | Fibre Ringlight_SB® Standard 600 µm, 1.8 mm | Laser : LumeSeal® Introducteur : Introducteur 6 Fr |
| RINGLIGHT® FIBER PROBE IRH_SB 1,0 mm CE 1639 | ORLF000005_SB | Fibre Ringlight_SB® Slim 400 µm, 1.0 mm | Laser : LumeSeal® Introducteur : Introducteur 4 Fr ou Cathlon 16G |
| RINGLIGHT® FIBER PROBE IR_SB 1,8 mm CE 1639 | ORLF000006_SB | Fibre Ringlight_SB® Fused Standard 600 µm, 1.8 mm | Laser : LumeSeal® Introducteur : Introducteur 6 Fr |
| RINGLIGHT® FIBER PROBE IRH_SB 1,3 mm CE 1639 | ORLF000007_SB | Fibre Ringlight_SB® Fused Slim 400 µm, 1.3 mm | Laser : LumeSeal® Introducteur : Introducteur 4 Fr ou Cathlon 16G |
b) Fibre laser Ringlight®
| Libellé | Référence | Spécifications techniques | Compatibilités |
|---|---|---|---|
| RINGLIGHT® FIBER PROBE IR 1,8 mm CE 1639 | ORLF000003 | Fibre Ringlight® Standard 600 µm, 1.8 mm | Laser : Endotherme™ 1470 Introducteur : Introducteur 6 Fr |
| RINGLIGHT® FIBER PROBE IRH 1,0 mm CE 1639 | ORLF000005 | Fibre Ringlight® Slim 400 µm, 1.0 mm | Laser : Endotherme™ 1470 Introducteur : Introducteur 4 Fr ou Cathlon 16G |
| RINGLIGHT® FIBER PROBE IR 1,8 mm CE 1639 | ORLF000007 | Fibre Ringlight® Fused Standard 600 µm, 1.8 mm | Laser : Endotherme™ 1470 Introducteur : Introducteur 6 Fr |
| RINGLIGHT® FIBER PROBE IRH 1,3 mm CE 1639 | ORLF000006 | Fibre Ringlight® Fused Slim 400 µm, 1.3 mm | Laser : Endotherme™ 1470 Introducteur : Introducteur 4 Fr ou Cathlon 16G |
c) Lasers et compatibilité
| Libellé | Référence | Spécifications techniques | Compatibilités |
|---|---|---|---|
| Laser LumeSeal® CE 1639 | ENDOV2_SB |
| Compatible avec fibres Ringlight_SB® |
| Laser Endotherme™ 1470 CE 1639 | PHARAON 1470 |
| Compatible avec fibres Ringlight® |
LSO Medical a su travailler avec les meilleurs fournisseurs afin de mettre à votre disposition tous les équipements et consommables complémentaires nécessaires à la réalisation des procédures laser :
| Libellé | Référence | Spécifications techniques | Compatibilités |
|---|---|---|---|
| Pompe DP 30 – Nouvag | 4187 |
| Tubulure Nouvag 6022 / 6022a / 6022b |
| Tubulure – Nouvag | 6022 / 6022a / 6022b | Longueur : 4 mètres | Pompe DP 30 – Nouvag |
| Kit d’introduction 6 Fr – SCW | INTRO6F03818GS |
| Fibre Ringlight® Standard |
À destination : des chirurgiens vasculaires, des médecins vasculaires, des pharmaciens, des ingénieurs biomédicaux et du personnel de bloc opératoire
Equipement médical Laser : Endotherme™ et LumeSeal_SB®. Classe DM : IIb. Classe Laser : 4 (port de lunettes de protection obligatoire)
Equipement consommable stérile : Ringlight® et Ringlight_SB®, Classe DM : IIa
![]() 1639
1639
Consommables Lasers : Les fibres Ringlight_SB® sont vendues stériles. Elles sont stérilisées à l’oxyde d’éthylène. Elles ont été conçues pour un usage unique exclusivement. Elles ne peuvent pas être réutilisées, ni être de nouveau stérilisées.
Dispositifs lasers endoveineux :
Usage prévu
Le dispositif LASER est utilisé pour produire une énergie laser avec des paramètres contrôlés (notamment longueur d’onde, puissance et mode d’émission) et pour l’acheminer vers un dispositif de sortie compatible, tel qu’une fibre optique endoveineuse, afin de permettre l’application contrôlée d’une énergie thermique au sein de la veine cible lors de procédures endoveineuses.
Le dispositif est utilisé sous guidage échographique et conformément aux instructions d’utilisation du fabricant.
Destination prévue
Le dispositif LASER est destiné à générer et délivrer une énergie laser à des fins thérapeutiques, pour une utilisation endoveineuse dans le cadre de la coagulation, de l’occlusion et de l’ablation des veines saphènes des membres inférieurs, chez des patients présentant une maladie veineuse chronique, lorsqu’un traitement thermique endoveineux est cliniquement indiqué.
Le dispositif est destiné à être utilisé chez des patients adultes par des professionnels de santé formés, dans un environnement médical approprié.
Indication d’utilisation
Le dispositif LASER est indiqué pour une utilisation dans des procédures de coagulation, d’occlusion et d’ablation thermique endoveineuse des veines saphènes, chez des patients présentant une insuffisance veineuse associée à un reflux veineux documenté.
L’indication repose sur une évaluation clinique et hémodynamique préalable, incluant un examen écho-Doppler, et sur la décision du praticien, conformément aux recommandations cliniques en vigueur.
Consommables stériles :
Usage prévu
La fibre optique endoveineuse est utilisée pour acheminer, diffuser et appliquer de manière contrôlée l’énergie laser au sein de la veine cible lors de procédures endoveineuses, conformément aux paramètres définis par le dispositif laser compatible.
La fibre est utilisée sous guidage échographique et conformément aux instructions d’utilisation du fabricant.
Destination prévue
La fibre optique endoveineuse est destinée à transmettre et diffuser une énergie laser, générée par un dispositif laser compatible, à des fins thérapeutiques, pour une utilisation endoveineuse dans le cadre de la coagulation, de l’occlusion et de l’ablation des veines saphènes des membres inférieurs, chez des patients présentant une maladie veineuse chronique, lorsqu’un traitement thermique endoveineux est cliniquement indiqué.
La fibre optique endoveineuse est destinée à être utilisée chez des patients adultes par des professionnels de santé formés, dans un environnement médical approprié.
Indication d’utilisation
La fibre optique endoveineuse est indiquée pour une utilisation dans des procédures de coagulation, d’occlusion et d’ablation thermique endoveineuse des veine saphène, chez des patients présentant une insuffisance veineuse associée à un reflux veineux documenté.
L’indication repose sur une évaluation clinique et hémodynamique préalable, incluant un examen écho-Doppler, et sur la décision du praticien, conformément aux recommandations cliniques en vigueur.
Bénéfices attendus : Les avantages du traitement au laser endoveineux sont : une réduction de taille ou une oblitération complète des varices traitées, et l’amélioration ou même la réduction des symptômes veineux. Le risque de complications des varices diminuera considérablement.
Contre-indication : Le LumeSeal_SB® ne doit pas être utilisé dans les cas suivants : Patients présentant des thrombus dans le segment veineux destiné à être traité, Patients présentant un anévrisme dans le segment veineux destiné à être traité, Patients souffrant de maladies vasculaires périphériques avec un indice de pression systolique cheville-bras en dessous de 0,9, Patients souffrant de thrombose veineuse profonde ou ayant des antécédents de thrombose veineuse profonde, Patientes enceintes, Patients souffrant d’une infection sur la zone à traiter, d’un herpès actif ou d’une autre infection virale, D’autres contre-indications peuvent éventuellement être indiquées par le praticien au moment du traitement.
Effets indésirables : À partir de la littérature analysée, il est possible de définir trois grandes classes d’effets indésirables pour la procédure d’occlusion de GVS par laser : Les effets indésirables dits fréquents (incidence < 50 %) : ecchymoses, douleurs et thrombose veineuse superficielle. Les effets indésirables dits rares (incidence < 5 % dans la plupart des études) : thrombose veineuse profonde, paresthésies, brûlure cutanée. Les effets indésirables exceptionnels (moins de 10 cas décrits) : paresthésie persistante, au-delà d’un an, et embolie pulmonaire.
Utilisation des dispositifs : Formation à l’utilisation du LumeSeal® : Par LSO Medical ou personnes habilitées par LSO Medical. Lire attentivement les instructions figurant dans le manuel utilisateur. Pour que le système soit conforme aux exigences définies, une calibration de l’appareil doit être effectuée, au moins une fois par an. Cette calibration doit être effectuée par un technicien agréé par LSO Medical ou par son distributeur local agréé.
Traitement endoveineux par laser : Pris en charge par l’assurance maladie
Fabricant de dispositifs médicaux
LSO Medical – Biocentre A. Fleming, Bât. D – 280 rue Salvador Allende – 59120 Loos, France
Fabricant de système et nécessaire
Distributeur et importateur des produits : SCW, NOUVAG
Nettoyage boîtier plastique, écran tactile : tissus humides et détergent désinfectant conformes aux Normes Européennes Microbiologiques : Bactéricide (EN 1040), Bactéricide en milieu sale (EN 1276), Actif contre Aspergillus fumigatus et actif contre Mycobacterium tuberculosis , Fongicide : (EN 1275) Actif contre HIV-1, HBV, Rotavirus, Herpès virus et BVDV (substitut du VHC).
Rebut : Le LumeSeal® contient des éléments qui nécessitent un recyclage spécifique. Le produit peut être repris par le fabricant ou tout organisme compétent.
Référence interne : 23/04/LSOMEDICAL/PM/001
Matériovigilance : Il convient de notifier tout incident grave survenu en lien avec le dispositif au fabricant et à l’autorité compétente de l’Etat membre dans lequel l’utilisateur ou le patient est établi.
Version : IM EMB – VA-fr – Avril 2023


